Real-space and real-time dynamics of CRISPR-Cas9 visualized by high-speed atomic force microscopy.
要旨
近年、遺伝子(ゲノム情報)を人為的に編集する(ゲノム編集)試みが世界中で行われている。
その中でも、CRISPR-Casシステムは幅広い分野で広く利用される技術である。
CPISPR-Casシステムでは、Cas9と呼ばれるDNA切断酵素が、DNAを指定された場所で切断する「はさみ」として、一方、短いRNA(ガイドRNA)が「案内役」としてはたらいている。Cas9は20塩基程度のガイドRNAに結合し、そのガイドRNAと相補配列を持つDNAを切断する。
ガイドRNAの配列は自由にデザインできるため、DNAの様々な部位を選択的に切断することが可能である。
Cas9のDNA切断メカニズムは、結晶構造解析などで進められてきたが、「スナップショット」である結晶構造解析から、実際にCas9がどのように構造変化するのかはわからなかった。
そこで、本研究では、高速AFMを用いることで一分子のCas9をリアルタイムで解析し、Cas9の詳細な動作機序を明らかにした。
Keyword: CRISPR-Casシステム
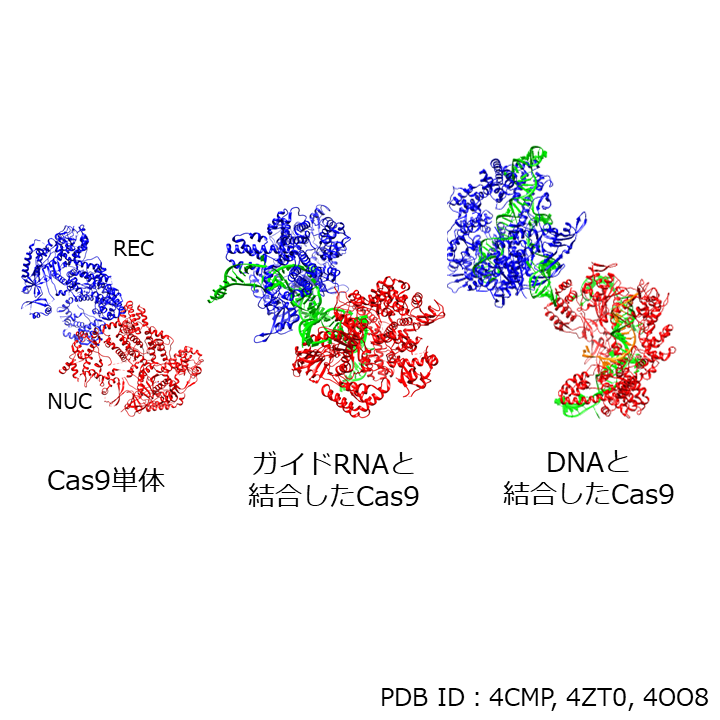
Cas9はDNAを認識するREC部位とDNAを切断するNUC部位の2つの領域からなるタンパク質である。
自然界においてCRISPR-Casシステムは原核生物がウイルス等の外敵から身を守るための免疫機構として機能している。
CRISPR-Casシステムの存在は古くから知られていたが、一部の微生物学者らが関心を寄せる程度であった。
しかし、2012年にCRISPR-Casシステムを利用した遺伝子の編集手法が考案され、その関心が爆発的に高まった。
”A Programmable Dual-RNA–Guided DNA Endonuclease in Adaptive Bacterial Immunity”
2020年には、この手法を開発したEmmanuelle Charpentier博士、Jennifer A. Doudna博士にノーベル化学賞が授与された。
観察結果
高速AFMでの観察の結果、ガイドRNAと結合する前のCas9は、時間とともにダイナミックに形を変えていて、「動きの大きな」構造をとっていることがわかった。
一方、ガイドRNAと結合したCas9は形状の変化が少なくなり、より安定な構造へと変化することが明らかになった。この構造変化により、DNA切断の活性を獲得すると考えられる。
さらに、Cas9がDNAに結合し、切断する一連の反応を可視化することにも成功した。
Cas9はDNA中の目的配列を探すとき、DNA上をスライドするのではなく、DNAとランダムな衝突を繰り返し、目的配列を探索することが初めて明らかになった。
さらに、Cas9と目的配列DNAとの結合がトリガーとなり、Cas9の一部が構造変化してDNAが切断される様子も確認された。
これらの知見は、CRISPR-Casシステムの理解に繋がるだけでなく、遺伝子編集技術の高度化に向けた基盤となることも期待されている。
関連するWebコンテンツのご紹介
下記リンクから動画等をご覧いただけます。
出典論文
Shibata M, Nishimasu H, Kodera N, et al.
Real-space and real-time dynamics of CRISPR-Cas9 visualized by high-speed atomic force microscopy.
Nat Commun. 2017;8(1):1430. doi:10.1038/s41467-017-01466-8
https://www.nature.com/articles/s41467-017-01466-8